Цефалоспориновые антибиотики применяются в клинической практике с начала 60-х годов и за эти годы синтезировано более 50 препаратов этой группы. (Periti P.J Chemother 1996) В настоящее время цефалоспорины занимают ведущее место при лечении различных инфекций в ветеринарной практике; в большинстве случаев им отдается предпочтение в схемах начальной эмпирической терапии инфекций различной локализации. В то же время ограничивающим фактором применения цефалоспоринов является развитие резистентности микроорганизмов в результате продукции ими бета-лактамаз.
Особенно эта проблема стала актуальна в последние годы из-за широкого применения цефалоспоринов, иногда неоправданного и часто бесконтрольного. Использование одних и тех же антибиотиков для лечения животных и людей должно быть ограничено.
Понижение эффективности антибиотиков, связано с нарушением правил использования антибиотиков, занижение дозы (однократное применение вместо двух или трехкратного в сутки). Использование цефтриаксона 1 раз в сутки при том, что концентрация этого препарата поддерживается в течение 16 часов. Однократное введение в блокаде не отменяет двух или трехкратное использование препарата в сутки. Если антибиотик применялся местно для блокады однократно, то с интервалом 8-12 часов он должен быть введен внутримышечно или внутривенно.
Также большее предпочтение в выборе препарата должно отдаваться препаратам с низкой токсичностью для макроорганизма.
Спектр действия препарата никак не связан с его токсичностью. Современные антибиотики: цефалоспорины 3 и 4 поколения, карбапенемы, защищенные пенициллины, обладают высокой терапевтической активностью, широким спектром действия и при этом минимальным токсическим действием на организм животного, в отличие от левомецитина, который при узком спектре действия и бактериостатическом эффекте весьма опасен для макроорганизма, поэтому данный препарат не используется и запрещен в большинстве развитых стран мира. Также ушло в прошлое использование в ветеринарной практике стрептомицина, канамицина, бицилина, наих заменили гораздо более безопасные, эффективные, с широким спектром действия препараты.
Процент устойчивых штаммов у стафилококков составляет: к бензилпенициллину – 80-95%, к тетрациклину – 70-85%, к левомицетину – 30-55%.
Следует уделить внимание способу введения антибиотика
Внутривенное или внутриартериальное введение может в ряде случаев быть эффективнее, чем внутримышечное введение того же антибиотика. А при инфекции в ЦНС интратекальное введение антибиотика эффективнее настолько, что другое использование их является неоправданным и формирование контрольной группы в медицине представляется на сегодняшний день не этичным.
Принципы рациональной антибиотикотерапии должны стать руководством для ветеринарных врачей всех специальностей. Эти принципы применимы для антибиотиков любой группы, в том числе цефалоспоринов.
Антибиотик должен избирательно подавлять жизнедеятельность патогенного микроорганизма, не оказывая существенного воздействия на гомеостаз организма пациента.
Для воздействия на инфекционно-воспалительный процесс антибиотик должен поступать в ткани очага в достаточной (минимальной подавляющей) концентрацией.
Назначение терапии должно осуществляться с учетом чувствительности возбудителя.
Начальная (эмпирическая) противомикробная терапия проводится с учетом органолептических свойств возбудителя, основывается на знаниях о наиболее вероятном микробном «пейзаже» гнойной раны.
Исходя из полиэтиологической теории, целесообразно проведение полиантибактериальной терапии препаратами с перекрывающими полями противомикробного спектра.
Дозы, путь введения, кратность введения противомикробного препарата должны основываться на необходимости создания в очаге воспаления минимальной подавляющей концентрации.
Назначение антибактериального препарата должно сопровождаться комплексной "терапией сопровождения" направленной на регуляцию тех звеньев гомеостаза, которые наиболее подвергаются агрессии данным препаратом (группой).
При проведении противомикробной терапии необходимо учитывать химиорезистентность микроорганизмов и включать в комплекс мероприятия, направленные на ее преодоление.
Антимикробная терапия должна состоять не только из собственного антибактериального средства, но и из мероприятий, направленных на создание условий неблагоприятных для жизнедеятельности микроорганизмов, и на уменьшение количества патогенов в ране.
Существуют органолептические ориентиры для выбора антибиотика до получения результатов лабораторных исследований. При получении из очага гнойного воспаления густого, сливкообразного гноя, предположительным возбудителем является стафилококковая флора. Наличие жидкого, зловонного гноя, некротизированных тканей в ране дает основание предполагать, что одним из участников микробной ассоциации является грамоотрицательная бациллярная флора. Если гной из раны не получен, при сдавлении краев раны выделяется в скудном количестве мутно-красноватая жидкость-это, вероятно, анаэробная микрофлора.
Так как цефалоспорины наиболее часто используются в ветеринарии, необходимо подробнее рассмотреть эту группу препаратов. В зависимости от спектра антимикробной активности цефалоспорины принято разделять на четыре поколения. Сравнительная характеристика различных поколений цефалоспоринов представлена в табл.1.
Таблица.1.
| Сравнительная активность in vitro цефалоспориновых антибиотиков |
| Поколения цефалоспоринов |
Активность в отношении |
Стабильность к бета-лактамазам |
| грамположительных бактерий |
грамотрицательных бактерий |
стафилококков |
грамотрицательных бактерий |
| Первое |
+++ |
+/- |
++ |
- |
| Второе |
++ |
+ |
++ |
+/- |
| Третье |
+ |
+++ |
+ |
+ |
| Четвертое |
++ |
+++ |
++ |
++ |
Цефалоспорины I
поколения характеризуются высокой активностью преимущественно в отношении грамположительных бактерий (стафилококков, стрептококков, пневмококков). Их активность в отношении грамотрицательных бактерий ограниченна (в основном E.coli, Salmonella spp., Shigella spp., P.mirabilis) в связи с тем, что препараты легко подвергались гидролизу бета-лактамазами.
Цефалоспорины II
поколения характеризуются повышенной (по сравнению с цефалоспоринами I поколения) активностью в отношении грамотрицательных бактерий, прежде всего Haemophilus infuenzae и большей стабильностью к бета-лактамазам; в то же время эти препараты сохраняют высокую активность в отношении грамположительных микроорганизмов. Ограничением применения препаратов II поколения является низкая активность в отношении некоторых грамотрицательных микроорганизмов (Enterobacter spp., Citrobacter spp., Serratia spp., P.rettgeri, Klebsiella spp., P.vulgaris) и природная устойчивость Pseudomonas spp. и Acinetobacter spp.
Цефалоспорины III
поколения (цефотаксим, цефтриаксон, цефтазидим, цефоперазон) обладают высокой активностью в отношении большинства грамотрицательных бактерий. Однако в последнее десятилетие наблюдается существенное повышение резистентности грамотрицательных микроорганизмов к цефалоспоринам III поколения, в основном за счет продукции ими бета-лактамаз различных типов и классов. Важный механизм резистентности обусловлен гиперпродукцией хромосомных бета-лактамаз за счет мутаций в регуляторных областях генома, приводящих к дерепрессии синтеза фермента. Другим важным механизмом резистентности микроорганизмов к цефалоспоринам является продукция плазмидных бета-лактамаз расширенного спектра (наиболее часто отмечается у штаммов Klebsiella spp. - примерно в 30%), гидролизующих все цефалоспорины III поколения, что определяет их клиническую неэффективность в этих случаях. Рутинные лабораторные методы оценки антибиотикочувствительности часто не выявляют этот механизм резистентности, и лаборатория может выдать врачу неправильный результат, что создает дополнительные сложности лечения этих инфекций.
Сложности в подборе эффективного антибиотика стимулируют поиск новых антибактериальных препаратов, которые, с одной стороны, позволили бы преодолеть проблему мультирезистентности грамотрицательных возбудителей инфекций, особенно продуцентов бета-лактмаз расширенного спектра, и, с другой стороны, обладали бы более высокой активностью в отношении грамположительных микроорганизмов. Этот поиск привел к созданию в середине 90-х годов новых цефалоспориновых антибиотиков, которые были отнесены к препаратам IV поколения - цефепим и цефпиром, цефкином (Кобактан для внутривенного использования).
Особенностью химической структуры молекулы цефалоспоринов IV поколения является наличие одновременно отрицательного и положительного зарядов. Цефемовое ядро антибиотиков несет отрицательный заряд. Четвертичный азот циклопентапиридиновой группы несет положительный заряд и придает молекуле биполярную структуру, которая обеспечивает быстрое проникновение антибиотиков через наружную мембрану грамотрицательных бактерий и соединение с пенициллинсвязывающими белками, что снижает вероятность их гидролиза бета-лактамазами, локализующимися в периплазматическом пространстве. Кроме того, положительный заряд служит проводником молекулы для нахождения благоприятной позиции в пориновом канале бактериальной клетки.
Аминотиазолин-метокси-иминогруппа, прикрепленная в 7 положении цефемового ядра, оказывает более выраженное действие на грамотрицательные микробы и придает устойчивость к бета-лактамазам.
Эти свойства цефалоспоринов IV поколения (быстрое проникновение через наружную мембрану бактерий, низкое сродство к бета-лактамазам и эффективное связывание с пенициллинсвязывающими белками) обеспечивают их активность в отношении грамотрицательных бактерий, в том числе штаммов, резистентных к цефалоспоринам III поколения.
У цефалоспоринов IV поколения широкий, хорошо сбалансированный антимикробный спектр. Они сочетают активность цефалоспоринов I-II поколения в отношении грамположительных микроорганизмов (метициллин-чувствительные стафилококки, стрептококки, пневмококки) и некоторых анаэробов с высокой активностью цефалоспоринов III поколения в отношении грамотрицательных бактерий (семейство Enterobacteriaceae, Neisseriaceae, Haemophilus influenzae, Moraxella catarrhalis, Pseudomonas spp., Acinetobacter spp.).
Активность цефалоспоринов IV поколения в отношении грамотрицательных бактерий не уступает или превышает таковую наиболее активных цефалоспоринов III поколения - цефотаксима и цефтриаксона и сравнима с активностью фторхинолонов и карбапенемов. Цефалоспорины IV поколения, так же как цефтазидим и цефоперазон, проявляет активность в отношении P.aeruginosa. (С.В. Яковлев1999 г).
Цефалоспорины IV поколения в большей степени, чем цефалоспорины III поколения, устойчивы к гидролизу бета-лактамазами, продуцируемыми грамотрицательными бактериями, в том числе расширенного спектра, в связи с чем они часто сохраняют активность даже в отношении штаммов, резистентных к цефалоспоринам III поколения.
Цефалоспорины IV поколения преодолевают механизм резистентности к цефалоспоринам III поколения, связанный с гиперпродукцией хромосомных бета-лактамаз.
Активность цефалоспоринов IV поколения в отношении стафилококков сравнима с активностью цефалоспоринов I и II поколений и превосходит активность цефалоспоринов III поколения.
Цефепим и цефпиром высокоактивны в отношении пневмококков, в том числе штаммов со сниженной чувствительностью к бензилпенициллину.
Однако цефалоспорины IV поколения, как и цефалоспорины других поколений, не активны в отношении метициллинрезистентных стафилококков. В данном случае следует расширить спектр действия антибиотиков ванкомицином.
Цефепим и цефпиром, цефкином(Кобактан для внутривенного использования) обладают определенной активностью в отношении некоторых анаэробов, однако они не действуют на наиболее частых возбудителей анаэробных инфекций брюшной полости и ран, поэтому в этих случаях, как правило, требуется сочетанное назначение с метронидазолом или клиндамицином, ванкомицином.
В многочисленных клинических исследованиях показана высокая эффективность цефалоспоринов IV поколения при лечении различных инфекций, в том числе наиболее тяжелых - пневмонии, перитонита, сепсиса, менингита, инфекций у пациентов с нейтропенией. После использования химиотерапевтических препаратов. (Beaucaire G. 1999).
Какими же в настоящее время представляются перспективы использования цефалоспоринов IV поколения в клинике?
Прежде всего, цефалоспорины IV поколения показаны для эмпирической терапии серьезных инфекций, учитывая их широкий антимикробный спектр и невысокий уровень резистентности микроорганизмов к этим препаратам. К таким инфекциям относятся пневмония тяжелого течения, сепсис, интраабдоминальные (в сочетании с метронидазолом), инфекции у пациентов после политравмы, нуждающихся в интенсивной терапии, инфекции у онкологических больных, инфекции мягких тканей после травмы, при гнойных отитах у собак (в сочетании с амикацином).
Другая важная область применения цефалоспоринов IV поколения - установленный высокий уровень резистентности к цефалоспоринам III поколения грамотрицательных бактерий, выделяемых в конкретном случае, прежде всего у Enterobacter spp., Serratia marcescens, а также других Enterobaсteriaceae (Е.Б. Гельфанд, Б.З. Белоцерковский, Е.А. Алексеева, Е.Ц. Цеденжапов, В.И. Карабак, Б.Р. Гельфанд, 1999-N11).
Стоимость суточной дозы цефалоспоринов IV поколения в нашей стране сопоставима со стоимостью большинства препаратов III поколения. Весьма существенным с этой точки зрения является кобактан для внутривенного использования. Недельная доза этого препарата менее затратна, чем использование цефтазидима или цефоперазона, и гораздо экономнее, чем использование медицинского препарата цефепима(максипима). Более того, цефепим и цефкином (кобактан) могут применяться для лечения смешанных аэробно-анаэробных инфекций (в сочетании с метронидазолом). На основании результатов контролируемых исследований, даже при тяжелых инфекциях, цефалоспорины IV поколения могут назначаться в режиме монотерапии.
В хирургии следует придерживаться следующих правил:
- введение антибиотиков должно начинаться не позднее, чем за 3 часа до разреза;
- применение препаратов менее чем за час не снижает риск развития осложнений;
- должна обеспечиваться достаточная концентрация (выше минимальной подавляющей концентрации) препарата в тканях операционной раны;
- период полувыведения антибиотика должен совпадать или превышать длительность операции;
- препарат должен обладать минимальными побочными эффектами.
Для этой цели хорошо подходит цефкином (Кобактан для внутривенного применения).
В неврологии при проникновении микроорганизмов в ткани мозга; при энцефалитах и открытой/закрытой черепно-мозговой травме проводится антибиотикотерапия препаратами, проникающими через гематоэнцефалический барьер. Выбор антибиотиков зависит от возбудителя заболевания и способности препарата проходить через гематоэнцефалический барьер (таб. 2).
Предпочтение должно отдаваться антибиотикам широкого спектра действия, обладающим бактерицидными свойствами и по возможности низкой токсичностью:
- цефалоспоринам III и IV поколения (цефтазидиму, цефепиму);
- карбопинемам (меронему, тиенаму);
- фторхинолонам (пефлоксацину).
Дозы цефалоспоринов должны составлять 40-50 мг/кг (2 раза в день, внутривенно).
Для лечения бактериального энцефалита, вызванного L.monocytogenes используются аминогликозиды(амикацин).
Как мы видим, цефалоспорины хорошо проникают через гематоэнцефалический барьер, исключением тут является цефоперазон.
Интратекально используют антибиотики: амикацин, карбапенемы, тазоцин(пиперациллин/тазобактам), таривид(офлоксацин), максипим, фортум, ванкомицин, диоксидин.
Таблица. 2. Способности антибиотиков проходить через гематоэнцефалический барьер
| Хорошо |
Хорошо проникают при воспалении |
Плохо проникают даже при воспалении |
Не проникают |
| Изониазид |
Азтреонам |
Гентамицин |
Клиндамицин |
| Пефлоксацин |
Амикацин |
Карбенициллин |
Линкомицин |
| Рифампицин |
Амоксициллин |
Макролиды |
|
| Ко-тримоксазол |
Ампициллин |
Норфлоксацин |
|
| Хлорамфеникол |
Ванкомицин |
Ломефлоксацин |
|
| |
Меронем |
Стрептомицин |
|
| |
Офлоксацин |
|
|
| |
Цефалоспорины 3- 4 поколения |
|
|
| |
Ципрофлоксацин |
|
|
С появлением цефкинома (Кобактана для внутривенных инъекций) область применения цефалоспоринов IV поколения значительно расширилось ввиду его гораздо большей доступности, чем цефепима. Цефалоспорины IV поколения в практике ветеринарных врачей нашей клиники используются после операций на позвоночнике, для премедикации у пациентов, которым требуется вмешательство на спинном, головном мозге. Широкий спектр и хорошая биодоступность Кобактана для внутривенных инъекций позволяют использовать его перед большинством проводимых в ветеринарии операций.
В нашей практике цефалоспорины IV поколения используются для лечения пациентов с тяжелой политравмой, с множественными переломами, разрывами внутренних органов (мочевого пузыря, отрывами уретры и у кобелей - предстательной железы).
У собак с открытой черепно-мозговой травмой использование цефалоспоринов IV имеет прямое показание, так как эти антибиотики хорошо проникают через поврежденный гематоэнцефалический барьер.
Клинический пример лечения гнойного отита, осложненного энцефалитом, у собаки породы шарпей
В клинику поступил кобель 3 лет с симптомами атаксии. Неврологическое обследование выявило атаксию центрального происхождения. Проведена магнитно-резонансная томография, поставлен диагноз «энцефалит».
Назначено лечение: манит внутривенно и цефтазидим внутривенно.
Лечение проводилось 14 суток. После этого проведена операция по удалению слухового прохода.
После операции продолжена терапия с использованием цефтазидима, однако гнойное выделяемое продолжало наблюдаться (рис 7). С целью расширения спектра действия данному пациенту был назначен Кобактан для внутривенных инъекций в дозе 25 мг/кг 2 раза в день внутривенно в течение 7 дней. Уменьшение и прекращение гнойного отделяемого наблюдалось в течение 1-2 дней (рис 8).
При внутривенном введении кобактана не отмечено аллергических реакций и других побочных эффектов.
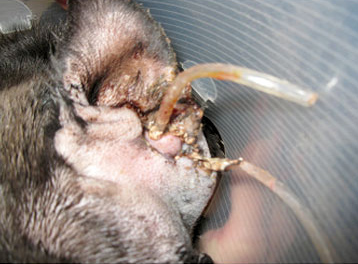
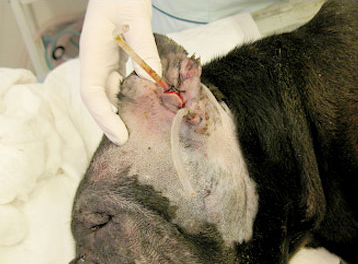 Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.
Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.
Рис. 8. Та же собака после замены цефтазидима на кобактан для внутривенных инъекций, наблюдается отсутствие гнойного отделяемого.
Таким образом, цефалоспорины IV поколения являются высокоэффективными и перспективными препаратами для лечения собак и кошек. Представляется рациональным более широкое внедрение и использование этих средств в клинической практике.


 Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.
Рис. 7. Кобель породы шарпей. После удаления слухового прохода наблюдается гнойное отделяемое, несмотря на использование цефтазидима.